CPS低値胃癌に対するニボルマブ併用療法の選択
実地臨床から見たCPS<5の胃癌に対するニボルマブ+化学療法の選択について
切除不能進行再発のHER2陰性胃癌一次療法におけるニボルマブ+化学療法の併用療法が承認されて、胃癌の治療は大きく塗り変わろうとしています。CheckMate-649およびATTRACTION-4の治療成績を見るとこのレジメンを使用しないという選択肢はなさそうに見えますが、しかしCPSが低い患者層に対する有効性については若干の疑問がまだ残るので、その辺りの治療判断をどうすべきかという議論がなされています。
最適使用推進ガイドライン(胃癌ニボルマブ2021年11月版)を見ると、CheckMate-649はCPS>5以外はPFSもOSもかなり微妙ではある pic.twitter.com/jmfzp0EBSw
— レ点.bot💉💊🧬 (@m0370) November 25, 2021
CPS低値の胃癌食道癌に対する免疫チェックポイント阻害剤上乗せの有効性は乏しい
そんな中で、Journal of Clinical Oncologyに興味深い論文が掲載されました。今回の胃癌のCheckMate-649の他に、胃癌のKEYNOTE-062と食道癌のKEYNOTE-590の3本の結果を統合して、KMsubtractionというRのパッケージを使ってCPS低値群だけの治療成績を算出しているものです。試験ごとにCPSのカットオフ値が若干異なるのですが、CheckMate-649はCPSが1-4を、KETNOTE-062やKEYNOTE-590はCPS 1-9をCPS低値と定義しています。ついでにCPS 0も含めた解析も行われています。
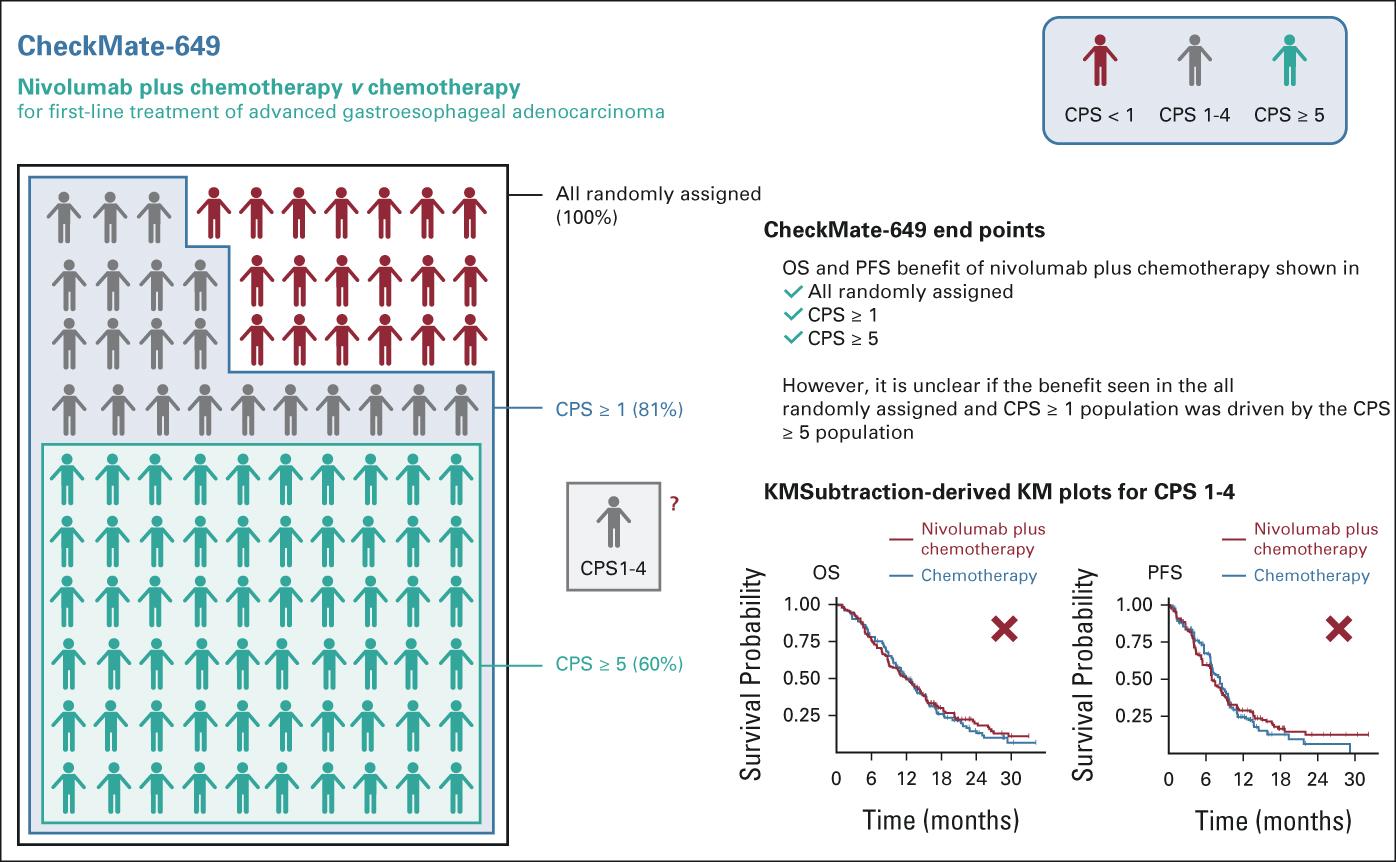
フォレストプロットそのものを見ていただくのが一番わかりやすいのですが図そのものを転載するのは(著作権的な意味で)ためらわれるので、ここでは数字のみ上げておくことにします。興味がある方は直接論文をご覧ください(今はフリーで閲覧できるようです)。
これを見ると食道癌のKEYNOTE-590だけはPFSでもOSでもCPS 9以下でも比較的ICI+化学療法の併用が良好な方にバーが偏っていますが(それでもぎりぎりHRは1を跨いでいる)、CheckMate-649とKEYNOTE-062はHRが0.9から1の間でいずれもほとんど差がなく、やはりCPS低値では免疫チェックポイント阻害剤の上乗せ効果は乏しそうです。
実際にはほぼ全例で一次治療にコンボを採用しそう
ただし上記のようにPD-L1 CPS低値でも、実際の診療ではよほど免疫チェックポイント阻害剤を使いにくい事情(自己免疫疾患の既往があるなど)がない限り、胃癌の一次治療にはニボルマブ+SOX/FOLFOXなどを採用することになりそうです。
安全性はあまり心配いらなそう
まず安全性の点で見てみます。SOX/FOLFOX療法にニボルマブを上乗せすることで当然いくらかの有害事象は増えますが、この数年で免疫チェックポイント阻害剤の使用経験がかなり増えたために、この治療を行う上でのリスク面の懸念はそれほど大きくないためです。治療開始後の比較的早期に重篤な下痢が起こった場合だけはS-1によるものかirAEなのかの見極めが重要ですが、それ以外の毒性については併用したからといってマネジメントが難しくなることはほとんど無さそうに見えます。
PFSやOSはともかくORRのメリットあり
次に有効性の点ではどうでしょうか。ATTRACTION-4でOSの差が付かず、CheckMate-649では前述の通りCPS低値群ではPFSもOSも曲線がかなり重なっているとはいえ、ORRはおよそ10%程度は高くなっています。最終的なOSで差が付かないORRにどの程度の意味があるのかという疑問は残るものの、デメリットが非常に小さく、いくらかの治療効果の上乗せがあるとすれば、実際の臨床現場では多くの場合はこちらの治療が選択されるだろうと予測します。
一次治療でニボルマブを使用しないCPS低値胃癌の後方治療
もう一つ、考えておかなければいけない点は一次治療でCPS低値を理由にニボルマブの上乗せをしなかった場合に三次治療以降の組み立てが難しくなる点です。
CPS低値なら三次治療をどうするのか?
三次治療のニボルマブ単剤のエビデンスになっているATTRACTION-2試験はCPS別の層別化解析の結果で治療を変えることをあまり想定していません。この試験だけを見れば、CPS低値であっても三次治療はニボルマブが第一選択になるように思われますが、例えばKEYNOTE-062などの結果を踏まえて考えると後方ラインでもやはりCPS低値では免疫チェックポイント阻害剤の効果はいくらか落ちると考えるのが妥当です。
ATTRACTION-2試験はプラセボに対しての優越性を示した試験ですが、その後にFTD/TPIが出てきて、また古くからの薬であるイリノテカンもあり、特にCPS低値という免疫チェックポイント阻害剤に不利な土俵で本当にニボルマブがFTD/TPIやイリノテカンに勝てるのかという疑問が残ります。
一次治療でニボルマブを使う方が後治療への移行率がスムーズ?
もちろん、CPS低値ではSOX→PTX+Ram→FTD/TPI→・・・と進めていくのも不可能ではありません。もしかするとCPS低値の人には奏効率の低いニボルマブで時間を消費するよりは細胞障害薬を中心に押し切るこちらの方が予後延長効果が高い可能性だってあります。しかし、いくらCPS低値だからといってニボルマブを使わないというほど腹をくくれるかというと実際にはそれはなかなか難しい。
となると、後方ラインで治療選択の迷いを無くすためにも免疫チェックポイント阻害剤は早い段階で試す、SOX/FOLFOXと併用するために時間を浪費することも心配しなくて良い、ということで一次治療に免疫チェックポイント阻害剤を上乗せするという選択肢がより現実的な選択肢に見えてきます。
CPSは測定すべきか問題
さて、どうせ一次治療でCPSが高値であれ低値であれニボルマブの上乗せを選択するのだとすれば、治療開始前のCPS測定は必要でしょうか。
治療方針に影響しないなら測定すべきでない?
治療方針の決定に影響しないのであれば、その検査は意味がないと言えるかもしれません。検査も貴重な医療費財源を使って行っていますので、無駄な検査は極力控えるべきという理屈には一定の説得力があります。治療方針が変わらないのなら、担当医の「CPSを知りたい」という好奇心だけのために検査の無駄打ちをすべきでないと言われれば、それはごもっとも。
CPSの結果を待つと治療開始が遅れる??
また、院内で検査が完結できる病理診断部門を備えている大学病院やがんセンターはともかく、おそらく市中病院ではCPS測定が外注検査になるところも少なくないでしょう。大腸癌で「確定診断もステージングも終わっているのにRAS/BRAFの検査結果だけがまだ出ない」ので1サイクル目は抗VEGF抗体も抗EGFR抗体も上乗せせずFOLFOX単独で治療開始し、抗体薬は2サイクル目から上乗せするという経験は多くの方がお持ちと思いますが、胃癌でも同じように「CPSの結果がまだ出ないので1サイクル目だけSOX単独で開始し、ニボルマブを上乗せするかどうかは2サイクル目から考える」となるのは煩雑でできれば避けたい。外注検査に時間をロスしてしまうのでCPSは測定しないというのも一理あります。
維持療法の選択がしやすくなる
一方で、CPS測定のメリットはどうでしょうか。一例として、ニボルマブの効果判定に役立つ可能性があります。例えば3サイクル後の効果判定CTで腫瘍縮小が認められたときに、SOXが効いたのかニボルマブが効いたのかがわからないことがありますが、CPS低値であればSOXが効いている可能性が高く、CPS高値(MSIも測定すればなお良い)であればニボルマブの効果かもしれません。有害事象が何もなければSOX+ニボルマブをずっと継続できた症例であっても、例えば何らかの有害事象で治療強度を下げて維持療法に移行せざるを得なくなったときに、S-1+ニボルマブにするのか、細胞障害薬はやめてニボルマブ単剤にするのかという判断の助けになります(当然CPS低値ならS-1+ニボルマブを、CPS高値ならニボルマブ単剤を選びやすくなります)。
特にSOX療法に比べてニボルマブを上乗せすればPFSが延びますから、普通にやれば今まで以上にオキサリプラチンが入る期間が長くなってしまいます。当然ながら末梢神経障害の発現率が高まると予想されますが、この末梢神経障害の発現が増えると二次治療のパクリタキセルが使いにくくなるという別の問題を引き起こします。したがって、有効性の高い一次治療が登場したからには、今まで以上に末梢神経障害出現時に適切に維持療法への移行時期を判断する必要が生じます。
なお、胃癌のSOX療法のオキサリプラチンの投与量は130mg/m2でレジメン登録している100mg/m2でレジメン登録している施設があるかと思います。大腸癌のSOX療法に準じれば130mg/m2ですが、国内では毒性の問題からG-SOX試験*1が100mg/m2で実施されていたためです。しかし、今回のニボルマブ併用療法の場合はATTRACTION-4に準じてオキサリプラチンの量は130mg/m2が標準となり、この点もオキサリプラチンの累積投与量増加に影響しそうです。
検査実施時には胃癌特有のheterogeneityに注意
胃癌のCPSを測定するための検体は内視鏡生検検体を用いることが多いかと思いますが、この際に胃癌では検体内のheterogeneityがあることに注意が必要です。これはHER2の評価でもしばしば言われることですが、内視鏡生検検体の場合は生検を行った場所によってHER2だけでなくCPSの値がぶれることが考えられます。したがって単回の生検でCPSを評価したとしてそれが本当に信頼できるのか(たまたま生検した場所によって結果が変動する可能性があるのではないか)ということを念頭に置く必要があります。
すなわち、CPS高値だからと言ってニボルマブのみの維持療法に早期に移行したり、逆にCPS低値だからといってニボルマブを使わないという判断が、もしかすると(たまたま生検した場所のCPSのぶれによって)患者に不利益をもたらしかねないというリスクを頭の片隅に置いておく必要があると言えそうです。
まとめ
胃癌の一次治療はニボルマブの承認によって大きく変わりました。そしてCPSというバイオマーカーはこれまで臨床試験では様々な解析に用いられていましたが、それがようやく保険診療でも行えるようになったことで、実際の現場での判断にそのデータを利用できるようになると同時に、パラメータが増えた分だけ難しい判断を迫られる局面が増えたと言えるでしょう。
しばらくは胃癌の治療に関するセミナーやディスカッションがリアルでもオンラインでも活発になされることと思います。様々な専門家の意見を聞いて、自分なりの判断根拠を確かなものにしてゆきたいと思います。
この記事に対するコメント
このページには、まだコメントはありません。
更新日:2021-12-13 閲覧数:1265 views.