胃癌のnabPTXの量は減らせるか問題
胃癌のナブパクリタキセル(nabPTX:アブラキサン)は骨髄抑制が強いから初回から減量されているケースがしばしば見られます。これに関するTwitterで見かけた会話が興味深かったので記録しておきます。
胃癌のnabPTX、骨髄抑制がPTXより強いから初回から減量開始してるって言う話をよく聞くけど、非劣性しか証明してないレジメンを初回から減量したら当然非劣性ですらなくなると思うんだけどその辺どう思ってるのかしら…。
— はなこっぴ (@hanacoppy) June 24, 2021
これまでの臨床試験での投与量は
もともと胃癌に対するパクリタキセル(PTA)の投与量はweeklyでは80mg/m2が、tri-weeklyでは210mg/m2が標準的です。tri-weekly PTXのほうが通院回数は減らせますが骨髄抑制が強く、おそらく多くの施設の実臨床ではweekly PTXが多用されているでしょう。WJOG 4007試験の結果では二次治療でのweekly PTXのOSは9.5ヶ月、PFSは3.6ヶ月、ORRは20.9%でした。

さて、nabPTXは第2相と第3相で結果が変わってしまったという薬の1つですが、ABSOLUTE試験の結果から現在はweekly nabPTXがweekly PTXに対する非劣性を示したレジメンとして考えられています。
国内第2相試験(NCT00661167)

第2相試験ではtri-weekly nabPTX(つまり3週間毎の投与法)が検討されましたが、このときの用量は260mg/m2です。1回あたりのかなり量が多く、Grade 3以上の好中球減少が49.1%、末梢神経障害が23.6%と有害事象も強く、正直なところ使いにくいレジメンです。
第3相ABSOLUTE試験
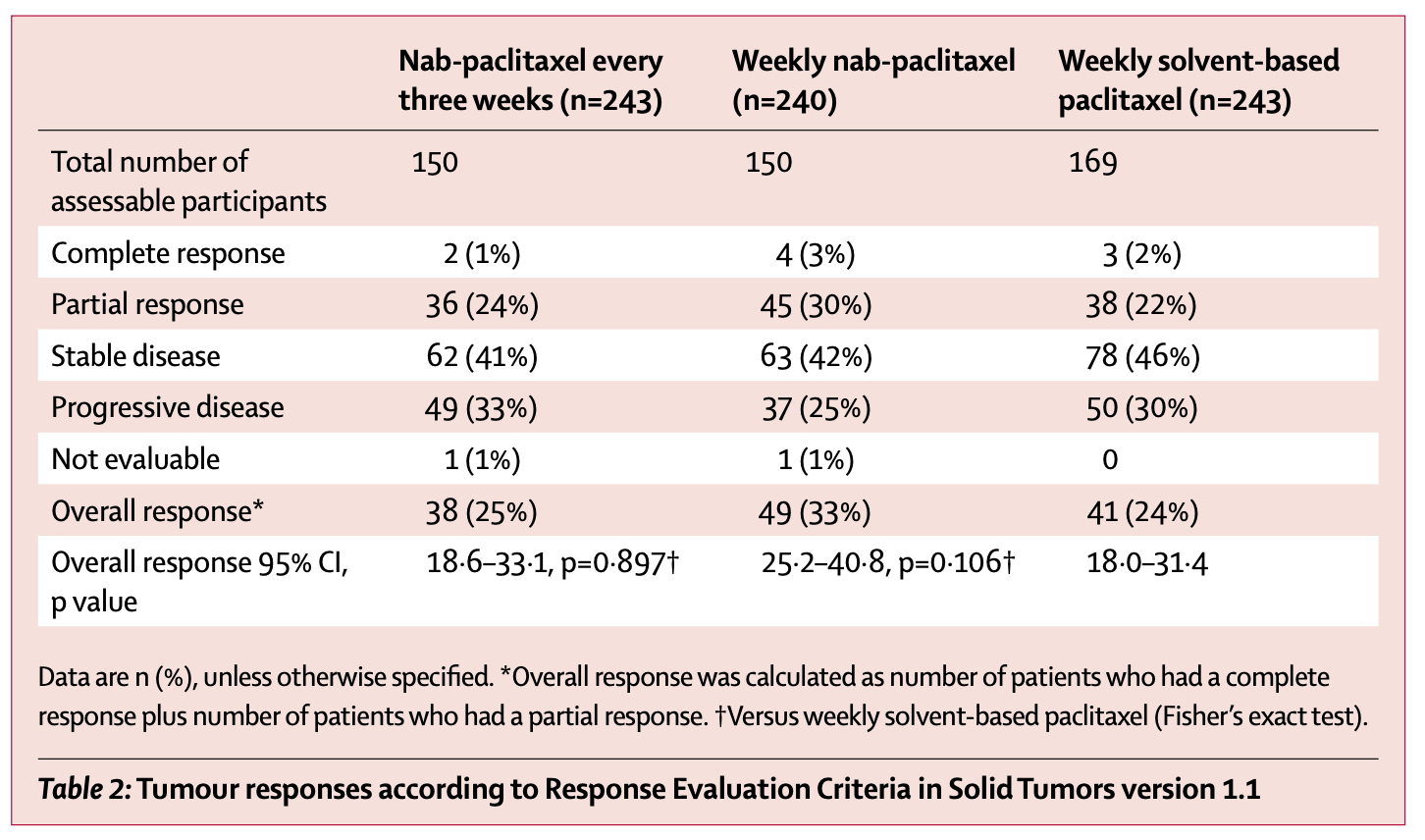
第3相試験ではweekly PTX 80mg/m2をコントロール群として、tri-weekly nabPTX(260mg/m2)とweekly PTX(100mg/m2)の3群での検討が行われています。つまり3週間毎投与法と毎週投与法の両方の群を設定しておき、tri-weekly nabPTX(260mg/m2)とweekly PTX(100mg/m2)はいずれもweekly PTX(80mg/m2)に対する非劣性を示そうとした試験です。

結果的にtri-weekly群は全体としてそう遜色ない成績を示していましたが事前設定の非劣性マージンを上回ってしまって非劣性を示せず(HR 1.06、CI: 0.87-1.31)、weekly nabPTXのみがweekly PTXに非劣性を示しました(HR 0.97、CI: 0.76-1.23)。OS、PFSはweekly PTXでわずかに長いものの、3群ともほぼ同等です。
ちなみに、ほぼ同等なんですがweekly nabPTX群がわずかに長く、有意な差でなかったにも関わらずメーカーが「OSが長い傾向にあった」とアピールしたもんだから一部の『コア層』から反発が起こりました。
tri-weekly nabPTXは第2相試験の結果を基に承認され、外来化学療法室の占拠時間が3週間に1度で60分のみという非常に短時間で済むために、外来化学療法室の混雑を緩和する切り札になると期待していたのですが、第3相試験の結果が発表されると一転して3週間毎の投与法はweekly PTXに対して非劣性を示すことができず、この使い方をすることができなくなりました。
第2相試験の結果で3週間毎投与法が既に承認され実地臨床で使用開始されていたため、多くの医師がズコー!とずっこけたそうな。
weekly nabPTXの減量を安易にやってしまうとよくなさそう
さしずめ、臨床試験でもRDIが80%くらいで非劣性だったから初回から減量してもいーんです😤といったところでしょうか?
— уон (@Yoh_tw) June 24, 2021
PTXは80mg/m2であったのに対してnabPTXは100mg/m2と単純に量が多く、その分だけ骨髄抑制のリスクも高くなりそうです。では、nabPTXをPTXと同様に80mg/m2に減量して実施すれば骨髄抑制の危険性を回避できるのでしょうか。
実はnabPTXの減量の可能性を模索した研究はいくつかあるようです。一つはOGSG1302試験。

もともとの第3相試験であるABSOLUTE試験は260mg/m2の3週毎投与だったのに対して、こちらの試験は1段階減量した220mg/m2で3週毎同様行っております。 これで末梢神経障害や骨髄抑制を大幅に軽減することが期待されますが、結果は惨憺たるもので、ORRはわずか3.1%でした。OSは6.3ヶ月、PFSは2.2ヶ月です。毒性はいくらか軽減されましたがこの奏効率では推奨することはとてもできなさそうです。
この結果を見る限り、全例を最初から減量して開始するというのはかなりナンセンスであると言わざるを得ません。いくら今はこれにラムシルマブを乗せることができると言っても、260mg/m2で実施した試験と220mg/m2で実施した試験でここまで結果が変わるのは驚きでした。
骨髄抑制が一定以上見られた症例のみRDIを下げるのはどうか
タキサン系抗腫瘍薬では 骨髄抑制が見られた症例の方が治療効果が高い事はいくつかの観察研究で示されています。これは骨髄抑制が強く出ている症例では血中濃度が高く保たれていることなどが関与していると考えられています。
そこで、骨髄抑制が見られた症例に限って累積投与量を減量することを許容するプロトコールで治療を行えば、相対的に少ない抗腫瘍薬投与量で治療効果が維持できるのではないかと考えたのがJACCRO GC-09試験です。

1サイクル目は標準的投与量のラムシルマブ(8mg/kg)とweekly nabPTX(100mg/m2)を投与します。そして、休薬や延期などの基準を満たした症例については2サイクル目からはnabPTXを隔週投与とするという、やや風変わりなプロトコルです。
JACCROのはたぶんJACCRO GC-09ですね。RAM+nabPTXでgr3の骨髄抑制が出たら減量ではなく1投1休に変更するやつ。まだ結果は出てないですよね?けっこう興味深い試験と思って注視してます
— レ点.bot💉💊🧬 (@m0370) June 24, 2021
この試験は症例集積が終了して現在は解析中のようで、結果はまだ出ていません。しかし、胃癌のRam+nabPTXにせよ膵癌のGEM+nabPTXにせよ、休薬・延期延期の繰り返しでなかなかスケジュール通りの投与ができず、減量減量を繰り返すことになってしまう症例では思い切って隔週投与にしてしまうとうまく治療が進むことがあるのも事実で、この臨床試験のプロトコルは非常に実地臨床に即したデザインになっていると感心しました。結果が出るのが楽しみな試験の1つです。
リアルワールドではどうなっているのか
国立がんセンター東病院がレトロスペクティブなデータとしてRam+PTXとRam+nabPTXの比較のデータを出されています。

これを見るとPTXの80mg/m2とnabPTXの100mg/m2は有効性にもほぼ差が無い一方で、同程度のRDI(減量率)で骨髄抑制の頻度もほとんど代わりがないので、nabPTXの100mg/m2がPTXの80mg/m2よりハイリスクとも一概にも言えなさそうな印象も受けます。裏を返せば、PTXの80mg/m2が投与できる人であればnabPTXは初回からむやみに減量せずとも100mg/m2で投与できそうだとも言えそうです。
ちなみに乳癌では
ちなみに乳癌では原文堅先生たちがtri-weekly nabPTXの減量の可能性についてABROAD試験で検討され、tri-weeklyの標準治療量である260mg/m2と、220mg/m2・180mg/m2に減量した群でランダム化比較した試験を実施され、すでに発表されています。

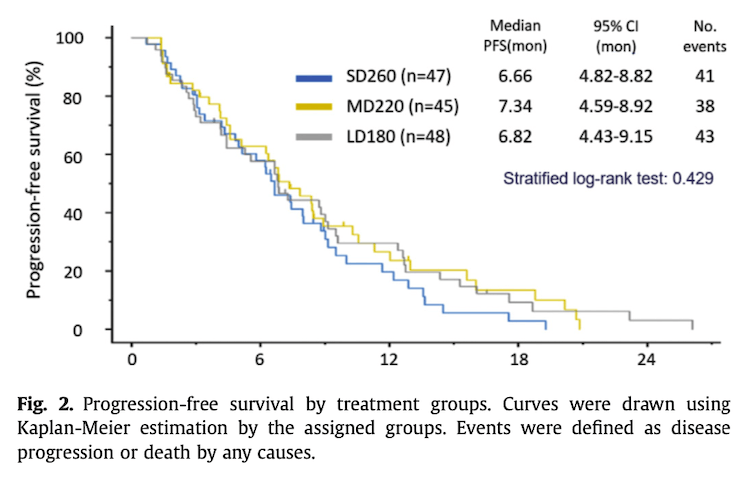
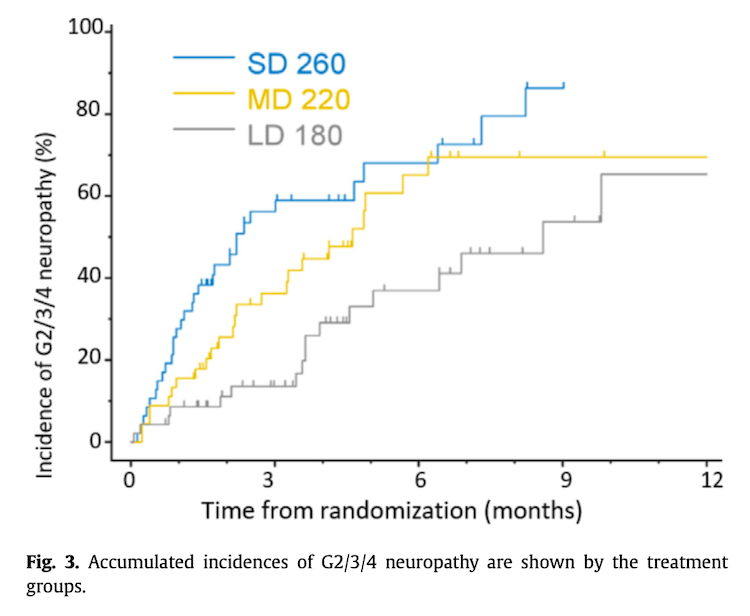
この結果を見ると、260mg/m2に対して220mg/m2や180mg/m2は比較的同程度の効果を保ちながらPFSはそれほど変わらない結果を示しています。標準治療量に対するRDI(relative dose intensity)はTable 5に出ていますように260mg群が0.87に対して220mgと180mgは0.77と0.63なので、やはり初回減量していると最終的なRDIが下がるようで、それにともなってGrade 3/4の末梢神経障害の出現率も下がっていますが、PFSの曲線がほぼ重なっているのは先ほどの胃癌のOGSG1302試験とは乖離した結果になっています。
これを見ると、乳癌のtri-weeklyでは減量開始という選択肢にもそれなりに根拠はありそうな印象ですね…。(胃癌ではそもそもtri-weeklyの260mgがABSOLUTE試験で80mgのweekly PTXに非劣性を示すこと自体ができていないので、この乳癌のABROAD試験の結果を胃癌に外挿することはできませんが。。。
まとめ
現時点では、nabPTXはABSOLUTE試験の結果からもわかるとおり、nabPTXは100mg/m2という量を投与してようやくPTXの80mg/m2に非劣性を示せていますし、最後に紹介した国立がんセンター東病院のデータを見てもやはりnabPTXは100mg/m2使ってようやくPTX 80mg/m2と同様のようです。
ようやく非劣性を示せているレジメンをさらにそこから安易に減量してしまうのであれば、はじめからnabPTXを選択する理由はなくPTXで十分になってしまいますから、nabPTXを使用するのであればやはり原則として100mg/m2を基準投与量として考えるべきだと言えそうです。
【PR】胃癌治療ガイドラインが2021年7月に改訂されます
2021年5月に3年ぶりに胃癌治療ガイドラインが改訂されて第6版になります。現在予約受付中のようです。

この記事に対するコメント
このページには、まだコメントはありません。
更新日:2021-06-26 閲覧数:1016 views.