複雑なPD-L1染色事情
PD-L1染色方法としてSP263と22C3のほかにSP142とか28-8とか色々あって、肺癌も乳癌も色々使い分けないといけないので非常に難しいですね。
ぼくは主に扱っている主戦場が消化器癌なので基本的にPD-L1の染色というのをプラクティスで実施することがなく(食道癌はペムブロリズマブの適応に関係しますが、ニボルマブがPD-L1関係なしに使えるのでペムブロリズマブ時代の出番がない)、PD-L1の染色方法についてあまりよく理解できていません。
最近出てきた例では
最近流れてきたツイートでは3期非小細胞肺癌の術後療法としてPD-L1陽性ならばアテゾリズマブがFDA承認されたとのニュースに、そのコンパニオン診断薬としてSP263を使ったVENTANA PD-L1 Assayが承認されたという話が付いていました。
FDA approved atezolizumab (Tecentriq, Genentech) for adjuvant treatment following resection and platinum-based chemotherapy stage II-IIIA NSCLC with PD-L1 expression on ≥1% of tumor cells. FDA also approved VENTANA PD-L1 (SP263) Assay as a CDx.#lcsmhttps://t.co/iwxIvZaCcY
— FDA Oncology (@FDAOncology) October 15, 2021
治療薬ごとのPD-L1染色方法の使い分け
PD-L1染色方法としてSP263と22C3のほかにSP142とか28-8とか色々あって、肺癌も乳癌も色々使い分けないといけないようになっています。PD-L1の判定方法が増えすぎて、ちょっと前の各種TKI毎にEGFR変異検出方法がバラバラだった時期を思い出します。
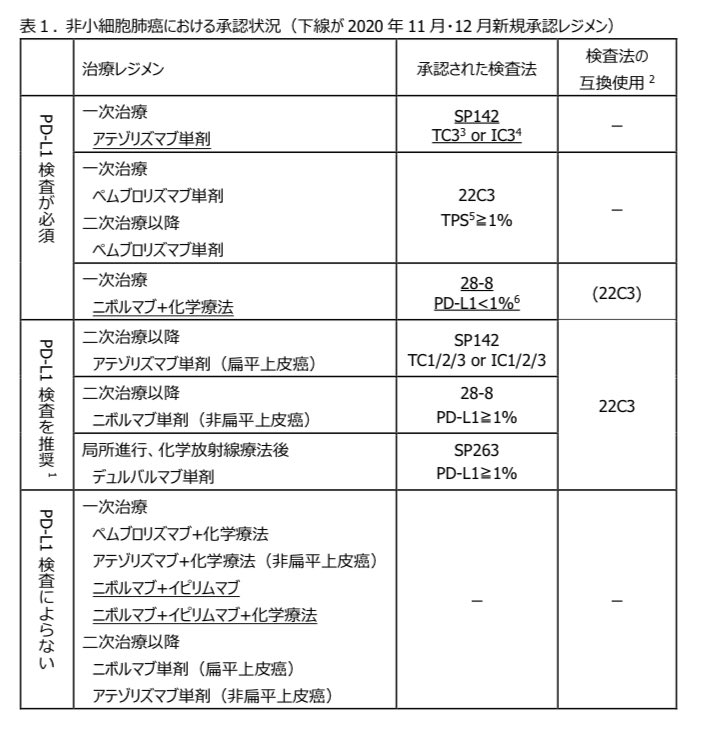
上記は「肺癌患者における PD-L1 検査の手引き第2版」の図ですが、乳癌や食道癌のPD-L1染色や、あるいは胃癌のCPS判定方法も勉強しておかなければならないことになって非常に複雑です。
そもそも免疫染色は施設間の格差もあることが知られていて、食道癌の臨床試験(KEYNOTE-181試験)の際にはPD-L1陽性率が非常に高い施設とほとんどない施設があることも問題視されていたように思います。
Ann Diag Pathol 41(2019):24–37. 一読。PD-L1抗体を多数使っていろんな組織を染めてみた報告。PD-L1は22C3, SP142の他にもSP263, 28-8などのcloneが多々ある。表現し難いほどにclone毎の染色性に差がある。これにプレアナリシス段階の施設間差が加わると恐ろしい。https://t.co/p2TAA6YjDL
— SAM_path🐀⚡️@病理医 (@SAM01859116) May 7, 2020
PD-L1 Blueprint Project
PD-L1の染色抗体による違いなどの差を埋めるために手をこまねいているわけでもなくて、PD-L1 Blueprint Projectという計画も進められています。

Blueprintの第1期では、28-8、22C3、SP263、SP-142などのPD-L1アッセイを比較してその同等性を検証しようとしました。癌細胞でのPD-L1発現の評価では28-8、22C3、SP263の3つが同等な分析性能を示したものの、SP-142 癌細胞の陽性率が低いという結果が得られ、また免疫細胞での一致率は高くないとの判断になったようです。
第2期でも25人の病理医が22C3、28-8、SP263の3つのPD-L1アッセイについて検討し、癌細胞の染色率が同等であるという結論になったようです*1。

自社のPD-L1評価方法をより使いやすい物にしようという競争も
またロシュがSP263を使ったPD-L1のデジタル計測システム「uPath PD-L1 (SP263) image analysis」を発表したりしていて、スキャンしたデジタルスライド画像を半自動的に評価するソフトウェアになっているようです。
できるだけ自社のPD-L1評価システムを使って欲しい(そしてその後に自社のモノクローナル抗体薬を処方してほしい)という狙いがありそうです。

Rocheが非小細胞肺癌におけるSP263抗体を用いた自動PD-L1検査アルゴリズムを発表。
— Kurono Emon (@chroemon) July 6, 2020
少なくともSP263を用いたPD-L1検査は、自動的にPD-L1の数値を算出してくれるようになるかも。EUだとSP263は22C3の代わりになるので、非小細胞肺癌のPD-L1検査全てが自動化される可能性もある。 https://t.co/WZvvKqa33t
現状では、性能同等であるからというだけでコンパニオン承認機能まで互換性が確保されているわけではないので結局は染色後に使いたい治療薬効補に応じて染色方法を変えざるを得ず、病理部門への人的・物的な負担がある程度かかってしまうという問題はまだ解決されていません。このあたりは、自社の抗PD-1/PD-L1抗体薬を使って欲しい製薬企業の思惑も絡んでくるので、解決には時間がかかるのでしょうかねぇ。
この記事に対するコメント
このページには、まだコメントはありません。
更新日:2021-10-17 閲覧数:1051 views.