リキッドバイオプシーに関するESMO推奨
リキッドバイオプシーの利用に関するESMOプレシジョンワーキンググループ推奨が公開されていた。ガイドラインという形にはなっていないがガイドライン的なもので、2022年8月版。われらが日本代表の吉野孝之先生(国立がん研究センター東病院)もグループのメンバーに入っている。
それぞれ中身は各自で見ていただくとして、自分で気になったところをメモしておく。
リキッドバイオプシーは重要な技術であるが組織パネルを完全に代替するには現時点では時期尚早
総論としては、進行癌のctDNA検査がかなり有用なのは確実であるということで一貫している。特に単塩基変異の検出では組織検体を用いたゲノムプロファイリングに比べて精度の遜色はなく、TAT(turnaround time:検査提出から結果返却までの所要時間)ですぐれるリキッドバイオプシーは今後さらに重要性が増してゆく。
しかし、各論ではリキッドバイオプシーの限界にも触れられている。特に、リキッドバイオプシーは偽陰性と偽陽性の問題が依然として組織検体を用いたパネル検査に比べて目立ってくるという点である。
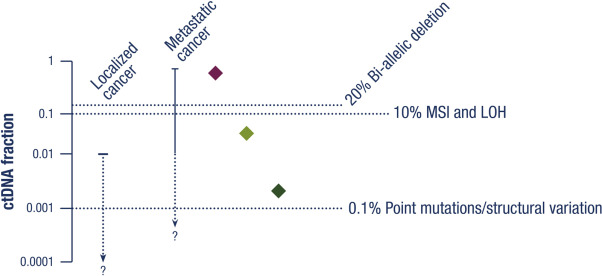
それぞれ様々な理由で生じ得るが、偽陰性の主な理由としては腫瘍由来DNAがあまりにも少なすぎるがために捉えられていない可能性があるという点が大きい。病変が小さすぎたり、肺転移や脳転移しかない場合はctDNAが検出されにくい。また有効な化学療法を継続中である場合は血中のctDNAも減衰するし、あるいは手術などの外科的侵襲が加わったあとは腫瘍以外の細胞損傷に由来するDNAが多く混入するために感度が下がってしまうという問題がある。染色体の融合・再構成やコピー数変化はまだctDNAは感度が低いなど、リキッドバイオプシーの原理に由来する問題もある。
偽陽性の理由としては、造血幹細胞のクローン性造血などに由来するCHIPの影響が大きい(CHIPの詳細についてはここでは言及しない)。CHIPかどうかは、KRASなど造血幹細胞でのクローンが稀な遺伝子では鑑別しやすいが、TP53やATMやCHEK2などDNA修復関連遺伝子でVAF 0.1〜5%の範囲のものをCHIPと腫瘍変異と鑑別するには現状はctDNAとWBC DNAの同時プロファイリング以外の方法で見分けることは現実的には不可と述べられている。
したがって、組織検体が入手可能で時間的余裕があるなら組織パネルを優先ということはこの提言では繰り返し述べられている。
その他に、再発早期発見などの微小病変検出はエビデンスが乏しい等、まだ発展途中の技術であることに留意が必要。
TMBの扱い
リキッドTMB(bTMB)は、FoundationOne CDxとFoundationOne Liquid CDxの使い分けの際にしばしば言及される大きなクリニカルクエスチョンになっている。
現状は組織TMBのようにICIのバイオマーカーとしては使用できない。bTMBはctDNA量により変動し、CHIPや腫瘍のサブクローンによって高く修飾され、また検体生成法の違いによってbTMBが組織TMBと相同性を持つか不明なので、カットオフ値をどうすべきか等も一定の見解がない。
これについては、リキッドバイオプシーを用いた免疫チェックポイント阻害剤の有効性に関する前向き報告のエビデンスが増えるのを待つしかないように思われる。
レポートの記載方法など運用面の問題にも言及
運用の問題にも言及されており、特にいままで国内の様々な学会や報告であまり言及されておらず目新しいなと感じたのはその記載方法に配慮が必要であるという点。具体的な例を挙げると、253頁に書かれた報告書式について、変異ctDNAが検出されない場合は「陰性」ではなく「不検出」と報告することが望ましい。また血漿DNA中のctDNA割合を測定できる場合はその割合を記載するなどで検体中にctDNA自体が十分量あったのかをわかるようにすることが望ましい。
不検出は常に偽陰性の可能性を頭におくということが、しつこいほどに繰り返して言及されている。
(そう考えるとF1 liquidでtumor fraction is not elevatedと記載されることは頻繁にあるが、あれは全部広い意味での「検査不成功」と考えても良いかも知れない。どれだけ偽陰性が含まれているかはわからないが、偽陰性があってもおかしくないという警告文に近い意味を持ちそう)
この記事に対するコメント
このページには、まだコメントはありません。
更新日:2022-08-31 閲覧数:628 views.